Como ya sabéis, los fenómenos de electrización empezaron a poner en entredicho la idea de Dalton de que el átomo fuese indivisible, por lo que a finales del S. XIX y principios de XX una serie de científicos comenzaron una serie de experimentos que le llevaron a descubrir las partículas subatómicas y más concretamente los protones y los electrones.
Thomson en 1897 estaba investigando con la conducción de la electricidad en los gases. En su experimentos utilizaba unos tubos alagados en los que introducía gas y en los cuales colocaba, a ambos extremos dos placas metálicas mediantes las cuales inducia las descargas eléctricas.
Thomson observó que cuando se inducían elevados voltajes dentro del tubo se producía una luminiscencia en la placa opuesta al tubo negativo, esto llevo a Thomson a pensar que debía existir algún tipo de partícula que fuese la responsables de esta luminiscencia. Thomson a estas partículas que debían viajar desde el electrodo negativo hacia el positivo le llamó Rayos Catódicos. Lo primero que se pregunto fue si estas partículas tenían masa y para ello colocó unas aspas en el centro del tubo y observo que estas se movían por lo que estas partículas tenían masa; lo segundo fue averiguar su masa y para ello colocó dos placas a ambos lados del tubo, más o menos en el centro, cada una con una polaridad para observar si las partículas tenían algún tipo de carga y observó que las partículas se desviaban hacia la placa de signo positivo por lo que dedujo que las partículas tenían carga negativa.
Estas partículas recibieron el nombre de electrones.
Unos años antes, 1886, Goldstein utilizando un tubo parecido a los que utilizaba Thomson, pero en los que el polo negativo tenía unas perforaciones. En este tuvo aparecían unas fluorescencias en el lado contrario al polo positivo, a las partículas que producían esta fluorescencia se les llamo rayos anódicos y poseen carga positiva. Debéis tener en cuenta que estas partículas no parten de los electrodos sino del gas del interior del tubo.
Estos experimentos llevaron a las siguientes conclusiones:
- El átomo es divisibles y está formado por partículas subatómicas.
- Los electrones tienen carga negativa.
- Los protones tienen carga positiva.
- En el átomo tienen que haber un número tal de electrones igual al de protones de tal forma que el átomo sea eléctricamente neutro.
Con esta afirmaciones Thomson propuso su modelo atómico el cual lo diseñó como una esfera con carga positiva y la cual contenía casi toda la masa del átomo y incrustados en ellas se encontraban los electrones en números tal que el átomo resultase eléctricamente neutro.
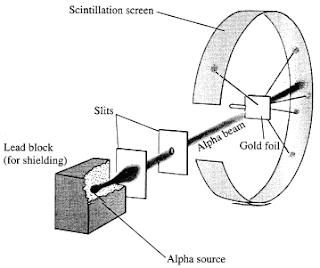
Más adelante en 1911, Rurtherford publicó su modelo atómico basándose en la siguiente experiencia:
Rurtherford bombardeo una lámina de oro con partículas alfa procedentes de un material radiactivo, tras el material situó una lámina sensible a las partículas alfa (ver dibujo). Rutherford observó que la mayoría de las partículas atravesaban la lámina de oro mientras que otras rebotaban. De las que atravesaban la lámina algunas pasaban rectas y muchas desviadas.
Basándose en esto Rurtherford postulo lo siguiente:
- El átomo tiene un núcleo central pequeño que concentra casi toda su masa formado por protones y neutrones; y que se encuentra cargado positivamente.
- Una corteza inmensa comparada con el núcleo donde giran los electrones y está cargada negativamente.
- El átomo al igual que en el modelo de Thomshon el átomo es eléctricamente neutro por lo cual el número de electrones es igual al número de protones.
El problema de este modelo es que los electrones al girar alrededor del núcleo van perdiendo energía con lo que caerían sobre el núcleo destruyéndose la materia, cosa que obviamente no ocurre.
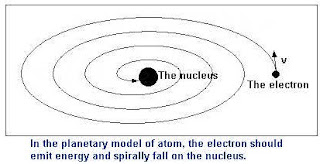
Debido a este problema N. Bohr formulo en 1913 unas modificaciones sobre el modelo atómico estableciendo los siguientes postulados:
- El electrón solo se puede mover por un orbital u órbita permitida, en la cual no emite energía, lo cual no solventamos el problema anterior.El electrón tiene una cantidad de energía que será mayor cuanto más alejada este la órbita del núcleo.
- El electrón sólo emite energía cuando salta de un estado mayor de energía hasta otro de menor energía, es decir cuando pasa de un orbital superior a uno inferior.